Roche erhält EU-Zulassung für Venclyxto-Kombinationen
Die EMA gibt grünes Licht für das Mittel Venclyxto (Venetoclax). Es wird im Kampf gegen neu diagnostizierte akute myeloische Leukämie angewendet.

Das Wichtigste in Kürze
- Die EU lässt das Mittel Venclyxto von Roche zu.
- Es wird in Zusammenarbeit mit AbbVie entwickelt.
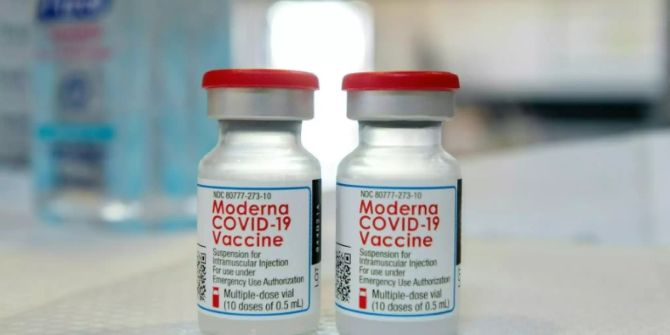
Der Pharmakonzern Roche hat für das Mittel Venclyxto (Venetoclax) die Zulassung in Europa erhalten. Nachdem sich der Ausschuss für Humanarzneimittel der Europäischen Arzneimittel-Agentur CHMP bereits positiv dazu geäussert hatte, kommt diese Entscheidung nicht überraschend.
Konkret geht es um den Einsatz von Venclyxto in Kombination mit einem Hypomethylierungsmittel zur Behandlung von erwachsenen Patienten mit neu diagnostizierter akuter myeloischer Leukämie (AML), die für eine intensive Chemotherapie nicht in Frage kommen, wie Roche am Dienstag mitteilte.
Wird von Roche und AbbVie entwickelt
Diese EU-Zulassung basiert laut Mitteilung auf den Ergebnissen der Phase-III-Studie VIALE-A und der Phase I/II-Studie M14-358.
In den USA ist Venclexta/Venclyxto in Kombination mit Azacitidin oder Decitabin oder niedrig dosiertem Cytarabin bereits zur Behandlung von neu diagnostizierter AML bei Erwachsenen zugelassen, die 75 Jahre oder älter sind oder Komorbiditäten aufweisen, die eine intensive Induktionschemotherapie ausschliessen.
Darüber hinaus ist Venclexta/Venclyxto in den USA und der EU auch bereits in anderen Kombinationen zur Behandlung von Leukämie zugelassen. Es wird von AbbVie und Roche gemeinsam entwickelt.
In den USA wird es von AbbVie zusammen mit der Roche-Tochter Genentech unter dem Markennamen Venclexta vermarktet. Und von AbbVie ausserhalb der USA.