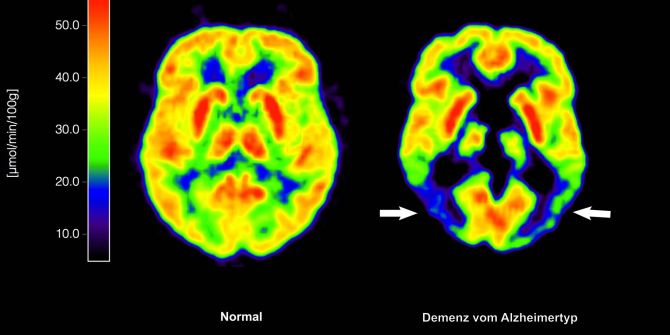
Alzheimer-Medikament Lecanemab hat keinen Zusatznutzen
Das Alzheimer-Medikament Lecanemab gilt als Hoffnung, doch das IQWiG bewertet den Nutzen für Frühstadien der Demenz skeptisch.
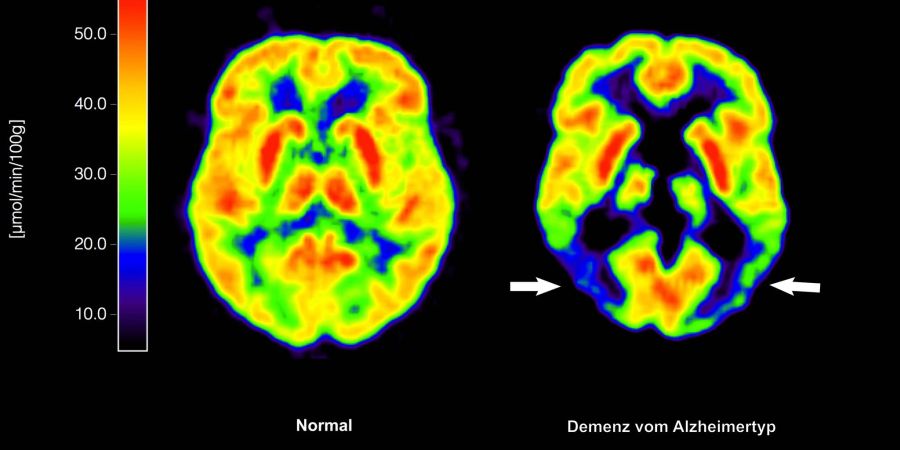
Das Alzheimer-Medikament Lecanemab wurde im April 2025 in der EU für die Frühbehandlung von Alzheimer zugelassen. Zudem ist es seit September in Deutschland erhältlich.
Lecanemab zielt auf die Amyloid-Plaques im Gehirn und soll das Fortschreiten der Erkrankung verlangsamen. So berichtet es die «Süddeutsche Zeitung».
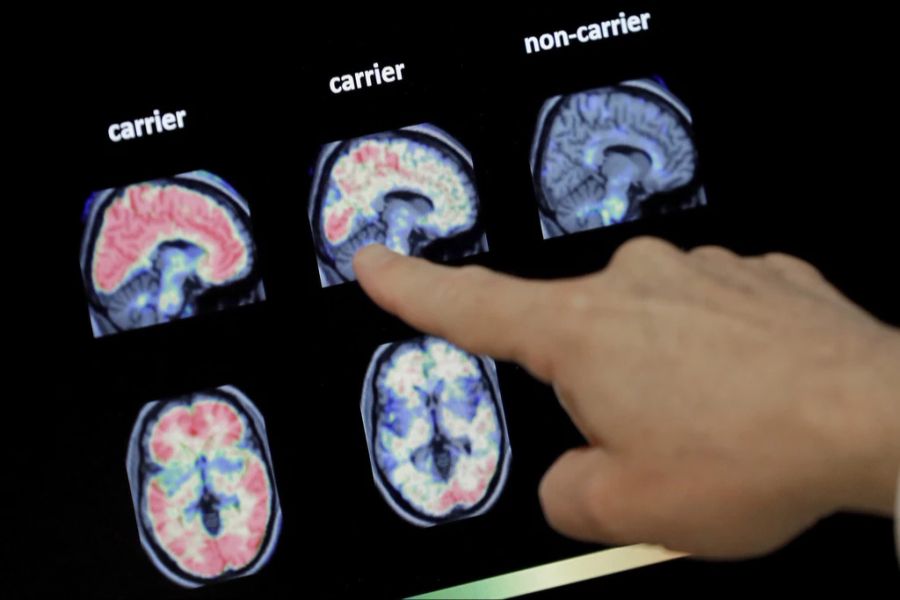
Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) veröffentlichte am 1. Dezember 2025 die erste Nutzenbewertung. Das Institut sieht keinen belegbaren Zusatznutzen von Lecanemab gegenüber bisherigen Therapien.
Alzheimer-Medikament birgt Risiken
Die leicht positiven Studiendaten reichten nicht aus, um einen Vorteil zu bestätigen, so die «Süddeutsche Zeitung». Experten kritisieren die Methodik des IQWiG.
Denn das Institut wählte nicht den Vergleich mit den Medikamenten, die in den Zulassungsstudien verwendet wurden.
Lecanemab birgt zudem auch Risiken. Nebenwirkungen wie Hirnschwellungen, Kopf- und Sehstörungen erfordern eine enge Überwachung der Patienten während der Therapie.
Donanemab ebenfalls beurteilt
Die Gesamtbewertung bleibt kontrovers, denn Lecanemab verlangsamt zwar den kognitiven Abbau um etwa 27 Prozent. Doch der Krankheitsverlauf wird nicht gestoppt.

Die Nutzenbewertung für ein ähnliches Medikament, Donanemab, läuft aktuell, Ergebnisse werden für Februar 2026 erwartet. Das IQWiG betont zudem, dass weitere Datennachlieferungen der Hersteller abgewartet werden.
Die Marktpreise könnten sich abhängig von der Zusatznutzenbewertung noch ändern, da Verhandlungen mit den Krankenkassen laufen. So berichtet es die «Pharmazeutische Zeitung» weiter.